

CONTACTO CON TUBERCULOSIS
Estudio de Contactos[B]
-
Generalidades
La tuberculosis (TBC) es un problema de magnitud mundial, que supone un reto para la medicina actual1,2,3,4,5. En la edad pediátrica existen dificultades añadidas como el mayor riesgo de progresión de infección a enfermedad, las dificultades en el diagnóstico (difícil aislamiento microbiológico y dificultad para distinguir entre infección y enfermedad) así como en el tratamiento debido a la falta de estudios en fármacos de segunda línea, en el cumplimiento terapéutico y a la escasez de formulaciones pediátrica1.
La OMS publicó en 2015 unas directrices sobre la atención a la infección tuberculosa latente (ITBL) dirigidas a los países de ingresos altos o medios donde la incidencia de TBC es menor de 100/100.000 habitantes2. En dicha publicación los niños y adultos en contacto con enfermos de tuberculosis pulmonar son uno de los grupos que presenta un beneficio claro en el estudio y tratamiento de ITBL2,3.
El riesgo de desarrollar TBC activa a lo largo de la vida tras el diagnóstico de ITBL es de un 5-10 %, y sobre todo se produce en los 5 años siguientes a la infección inicial; siendo mayor en los menores de 5 años por su mayor riesgo de progresión a enfermedad y a la aparición de formas meníngeas. El riesgo de progresión depende sobre todo del estado inmunitario del paciente2.
En España la incidencia de enfermedad tuberculosa fue de 10 /100.000 habitantes según el último informe del ISCIII5. El ISCIII en sus últimos informes (2014/2015) recomienda la investigación en poblaciones con mayor incidencia y optimización de los estudios de contactos sobre todo en los menores de 5 años por su mayor riesgo de progresión a enfermedad y a la aparición de formas meníngeas5
-
Estudio de contactos
El estudio de contactos se realiza en cada comunidad, según protocolos establecidos desde los servicios de epidemiologia y medicina preventiva. Y son estos últimos, los responsables de llevar a cabo el estudio de contactos. Como pediatras de atención primaria realizaremos el estudio en nuestra población y colaboraremos en todo lo necesario.
El estudio de contactos está indicado tanto si el caso con enfermedad tuberculosa es un adulto como si es un paciente pediátrico. El objetivo en esta situación es encontrar el caso índice y otros posibles casos infantiles derivados de ese caso índice4.
VALORACIÓN DEL CONTACTO[D]
PRIORIZACIÓN DEL ESTUDIO[E]
¿PROFILAXIS?[I]
TABLA 1: Determinación del periodo de contagiosidad. (Tomada de Guía práctica sobre el diagnóstico, tratamiento y la prevención de la tuberculosis MMSS 2011.) 4
|
Síntomas de tuberculosis |
Baciloscopia de esputo positiva |
Lesión cavitada en radiografía tórax |
Periodo de infecciosidad mínimo a considerar |
|
Presentes |
Sí/No |
Sí /No |
Tres meses antes del inicio de síntomas o de la sospecha consistente de tuberculosis |
|
Ausentes |
Sí |
Sí |
Tres meses antes del primer hallazgo diagnostico compatible con tuberculosis |
|
Ausentes |
No |
No |
Cuatro semanas antes de la fecha del diagnostico |
Adaptado de Center for Disease and Prevention. Guidelines for the investigation of contacts of persons with infectious tuberculosis; recommendations from the National Tuberculosis Controllers Association and CDC, and Guidelines for using the Quantiferon-TB Gold test for detecting Mycobacterium tuberculosis Infection, United states. MMWR 2005 Dec 16;54(RR-15): 1-55(174)
TABLA 2: Priorización del estudio de contactos de pacientes con tuberculosis pulmonar, laríngea, traqueal o endobronquial con baciloscopia de esputo positiva o lesiones cavitadas en la radiografía de tórax. (Modificada de Guía práctica sobre el diagnóstico, tratamiento y la prevención de la tuberculosis MMSS 2011)4.
|
SITUACIÓN |
PRIORIDAD |
|
Contactos primer círculo (Figura 1). Domiciliario-íntimo diario |
ALTA |
|
Contactos de edad < 5 años |
ALTA |
|
Contactos con factores de riesgo* |
ALTA |
|
Contactos en instituciones cerradas |
ALTA |
|
Contactos en personas entre 5-15 años |
MEDIA |
|
Contacto menos frecuente- segundo círculo (Figura 1). |
MEDIA |
|
Cualquier contacto no clasificado como de prioridad alta o media |
BAJA |
*Infección por HIV, diabetes mellitus, insuficiencia renal crónica, neoplasias hematológicas y de cabeza o cuello.
TABLA 3: Priorización del estudio de contactos de pacientes con tuberculosis laríngea, traqueal o endobronquial con baciloscopia de esputo negativa y radiografía de tórax sin lesión cavitada. (Modificada de Guía práctica sobre el diagnóstico, tratamiento y la prevención de la tuberculosis MMSS 2011) 4.
|
SITUACION |
PRIORIDAD |
|
Contactos de edad < 5 años |
ALTA |
|
Contactos con factores de riesgo* |
ALTA |
|
Contactos de primer círculo. Domiciliario -intimo diario. (Figura 1). |
ALTA |
|
Contactos en instituciones cerradas |
MEDIA |
|
Cualquier contacto no clasificado como de prioridad alta o media |
BAJA |
*Infección por HIV, diabetes mellitus, insuficiencia renal crónica, neoplasias hematológicas y de cabeza o cuello.
-
Valoración del paciente
Es prioritaria la valoración del paciente que nos consulta, para detectar los casos sintomáticos que precisen estudio rápido y completo de enfermedad tuberculosa por presentar clínica compatible: tos, adenopatías, fiebre, sudoración, anorexia, pérdida de peso o signos de hipersensibilidad tuberculínica (eritema nodoso y conjuntivitis flictenular).
Considerar el ingreso para estudio URGENTE si la clínica es compatible y no se pueden realizar las pruebas complementarias de forma ambulatoria
-
Valoración del contacto
Ante una familia que acude refiriendo contacto con un enfermo de tuberculosis tenemos que investigar:
D1. Datos del caso índice
- Localización de enfermedad:
- Contagiosa si pulmonar, laríngea, traqueal o endobronquial: Indicado realizar estudio de contactos
- No contagiosa si otras localizaciones: No está indicado realizar estudio de contactos
- Resultado de las pruebas microbiológicas:
- Baciloscopia: Positiva establece prioridad. Importante conocer la fecha de la última baciloscopia positiva
- Cultivo: Sensibilidad de la cepa índice
- Radiografía de tórax del caso índice: lesión cavitada, establece prioridad.
- Demora diagnóstica: tiempo transcurrido desde el inicio de los síntomas hasta el diagnostico (sospecha o certeza). (Tabla 1)
- Fecha de inicio del tratamiento antituberculoso
D2. Tipo de contacto:
Sistema de círculos concéntricos contemplando cada caso de forma individual4. (Figura 1). Según el ámbito donde haya tenido lugar el contacto (escolar, familiar o en “centro lúdico”), y según las horas diarias de contacto, hay 3 tipos de contacto:
- Intimo: diario, más de 6 horas al día
- Frecuente: diario, menos de 6 h al día
- Esporádico: No diario
D3. Situaciones especiales de los contactos que confieren riesgo y establecen prioridad
- Enfermedad de base que cause inmunosupresión
- Tratamientos inmunosupresores
- Edad < 5 años
-
Priorización del estudio de contactos
Tras averiguar los datos del caso índice y el tipo de contacto (D) se investigará según el orden de prioridad establecido. (Tabla 2 y 3):
- Prioridad alta: Estudio inmediato a realizar en 5-10 días
- Prioridad media: Realizar estudio en 10 días
- Prioridad baja: Solo realizaremos estudio si se detecta alta tasa de infección o enfermedad tuberculosa en contactos de más prioridad2
-
EXPOSICION TUBERCULOSA. Fundamentos de la profilaxis primaria / tratamiento de contactos
Definición: Exposición a tuberculosis sin signos de infección con primer Mantoux o IGRA negativo
No existe un acuerdo sobre la profilaxis primaria en estos casos. La mayoría de los autores proponen iniciar tratamiento, dado el mayor riesgo de desarrollar enfermedad durante el periodo ventana en:
- Menores de 5 años.
- Pacientes inmunodeprimidos (tratamientos inmunosupresores, comorbilidades, inmunodeficiencias) de cualquier edad.
En el resto de los pacientes puede obviarse el tratamiento, manteniendo una estrecha vigilancia hasta la realización del segundo Mantoux o IGRA6 .
La profilaxis primaria se realiza con isoniacida (INH) a 10mg/kg/día (dosis máxima: 300mg) + piridoxina hasta repetir el Mantoux a las 8-12 semanas, puesto que el periodo ventana oscila entre 4-12 semanas:
- Si este es negativo (<5 mm) se suspenderá el tratamiento en aquellos en los que se había iniciado. Aunque sea negativo, en menores de 3 meses o inmunodeprimidos con contacto de alto riesgo se aconseja completar tratamiento de ITBL6 (P) por ser pacientes de alto riesgo en los que el valor del Mantoux tiene bastantes limitaciones.
- Si es positivo (>5 mm) se continuará con la evaluación del paciente, realizando una radiografía de tórax (N).
FIGURA 1: Sistema de círculos concéntrico y lugar de contacto 4
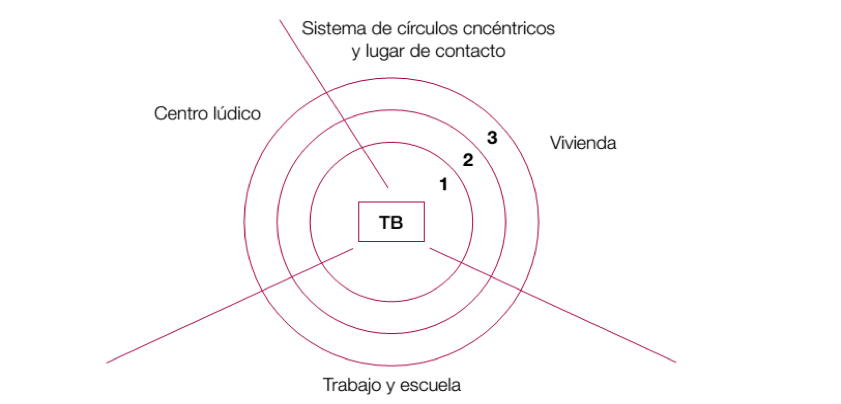
Tabla 4: Técnica de Mantoux o prueba cutánea con PPD
|
Técnica de Mantoux o Prueba cutánea con PPD |
|
TABLA 5: Dinteles de positividad de la prueba de Mantoux en nuestro medio. (Adaptada del documento de consenso de SEIP. Diagnóstico de la tuberculosis en la edad pediátrica) 5
|
INDURACIÓN ≥ 5 mm |
|
|
INDURACIÓN ≥ 10 mm |
|
TBC: tuberculosis; BCG bacilo Calmette-Guerin; VIH : virus de la inmunodeficiencia humana
-
Mantoux positivo
Debido al alto riesgo de infección y de progresión a enfermedad en la edad pediátrica e independiente de haber recibido la vacuna del bacilo Calmette-Guerin (BCG), en el estudio de contactos se considera positiva una induración ≥ 5 mm. La presencia de vesículas o necrosis son muy sugestivas de infección.
En pacientes inmunodeprimidos cualquier grado de induración se considera positivo y por tanto una vez descartada la enfermedad realizaremos quimioprofilaxis completa.
En nuestro medio y según el consenso publicado por la SEIP y SENP EN 2010 se establecen dos puntos de corte. (Tabla 5) 1.
Falsos positivos: vacunación previa con BCG, exposición a micobacterias no tuberculosas (MNT), infección o hematoma en zona de inoculación, alergia a otros componentes del PPD. En estos casos se debe realizar un IGRA.
Efecto booster: se produce en los vacunados con BCG, infectados por MNT y en las infecciones antiguas. En estos supuestos, cuando se realiza una PT, pueden reaccionar por debajo del dintel de positividad y se consideran negativos, pero los antígenos inyectados estimulan la memoria inmunológica por lo que al practicar una segunda prueba, pasados unos 7 días desde la primera, la reacción es positiva y el individuo puede ser catalogado erróneamente como conversor por infección reciente. Para obviarlo, se sugiere que cuando se pase de una induración menor de 10mm a una mayor de 10mm, se considerará que existe una infección tuberculosa latente (ITBL) si la segunda PT es 6mm o más superior a la primera PT.
-
Mantoux
En nuestro país la prueba de elección para el estudio de contactos sigue siendo la prueba de la tuberculina (PT), mediante técnica de Mantoux. (Tabla 4)
Esta técnica se basa en la reacción de hipersensibilidad retardada producida ante los antígenos del preparado derivado proteico purificado (PPD). De forma indirecta nos indica exposición, porque no existe ninguna prueba que diagnostique de forma directa la infección tuberculosa. No existen contraindicaciones para su realización4.
-
Mantoux negativo1,4,6
Debido al alto riesgo de infección y de progresión a enfermedad en la edad pediátrica, en estudio de contactos sólo se consideran negativos aquellos que presenten una induración < 5 mm, excepto en pacientes inmunodeprimidos en los que cualquier grado de induración se considera positivo.
En un estudio de contactos debemos de ser extremadamente cuidadosos y valorar otras opciones (repetir Mantoux, IGRAs, etc.) antes de excluir definitivamente el diagnóstico.
Falsos negativos
- Factores relacionados con el huésped:
- Tuberculosis diseminada o que afecte a serosas (miliar, meningitis)
- Tratamientos inmunosupresores (tratamientos biológicos, inhibidores TNF e IL y corticoides)
- Lactantes
- Malnutridos
- Vacunaciones recientes en últimos 3 meses con vacunas de virus vivos atenuados: triple vírica, varicela y polio oral
- Infección reciente por HIV, sarampión, paperas, varicela, tos ferina, fiebre tifoidea, brucelosis, blastomicosis.
- Enfermedades que cursan con inmunosupresión: neoplasias, sarcoidosis, insuficiencia renal crónica, inmunodeficiencias, cirugía mayor y grandes quemados
- Infección muy reciente: periodo ventana que oscila entre 4-12 semanas
- Factores relacionados con la técnica
- Conservación deficiente
- Técnica defectuosa
ENFERMEDAD TUBERCULOSA
TRATAMIENTO[R]
SEGUIMIENTO[S]
|
SITUACIÓN |
PRIORIDAD |
|
Contactos primer círculo (Figura 1). Domiciliario-íntimo diario |
ALTA |
|
Contactos de edad < 5 años |
ALTA |
|
Contactos con factores de riesgo* |
ALTA |
|
Contactos en instituciones cerradas |
ALTA |
|
Contactos en personas entre 5-15 años |
MEDIA |
|
Contacto menos frecuente- segundo círculo (Figura 1). |
MEDIA |
|
Cualquier contacto no clasificado como de prioridad alta o media |
BAJA |
|
SITUACION |
PRIORIDAD |
|
Contactos de edad < 5 años |
ALTA |
|
Contactos con factores de riesgo* |
ALTA |
|
Contactos de primer círculo. Domiciliario -intimo diario. (Figura 1). |
ALTA |
|
Contactos en instituciones cerradas |
MEDIA |
|
Cualquier contacto no clasificado como de prioridad alta o media |
BAJA |
Tabla 6 Dosis recomendadas de los fármacos antituberculosos de primera línea más empleados en edad pediátrica6
|
Dosis en pautas diarias, mg/kg/d (rango de dosis) |
Dosis máxima diaria (mg) |
|
Isoniacida 10 (7-15) a,b |
300 |
|
Rifampicina 15 (10-20)a |
600 |
|
Pirazinamida 35 (30-40) |
2.000 |
|
Etambutol 20 (15-25)c |
2.500 |
|
Estreptomicina 15-20 |
1.000 |
- La dosis más altas de isoniacida y rifampicina se utilizan en meningitis tuberculosa.
- Asociar piridoxina 15-50 mg/día (máximo 50 mg/día) si lactancia materna exclusiva, vegetarianos, alteraciones nutricionales, VIH y adolescentes gestantes.
- Se recomienda que durante el periodo de inducción de la enfermedad se utilice etambutol a dosis más bactericidas (20-25 mg/kg/día) y durante el periodo de mantenimiento disminuir a 15-20 mg/kg/día.
Excepcionalmente pueden considerarse pautas intermitentes de 3 días semanales con incremento de dosis, siempre con tratamiento directamente observado.
Tabla 7. Tratamiento de la tuberculosis extra pulmonar
|
Forma clínica de TB |
Tratamiento y duración |
Corticoides (dexametasona o prednisona) |
Tratamiento quirúrgico |
|
Afectación del SNC (meningitis, tuberculomas cerebrales) |
H 12 m + R 12 m + Z 2m + E/aminoglucósido |
Recomendado, durante 4-8 semanas |
Drenaje ventricular externo si hay hidrocefalia a tensión o progresiva. Posteriormente, válvula de derivación ventrículo-peritoneal si fuera necesario. Cirugía en caso de tuberculomas que no respondan al tratamiento, o que provoquen hipertensión intracraneal o abscesos |
|
Diseminada: TB pulmonar miliar, TB que afecta a más de 2 órganos no contiguos o aislamiento MBT sangre/orina |
H 6-12 m + R 6-12 m + Z 2 m + E/aminoglucósido |
Recomendado si hay hipoxemia, afectación endobronquial o del SNC |
|
|
Espinal |
H 6 m-9 m + R 6 m-9 m + Z 2 m +E/aminoglucósido |
Recomendado en compresión medular y valorar 12 m de tratamiento |
Si inestabilidad espinal o evidencia de compresión medular |
|
Ganglionar No prolongar tratamiento de TB ganglionar en caso de supuración o fístula |
H 6 m + R 6 m + Z 2 m + E/aminoglucósido |
Recomendado si signos inflamatorios de compresión |
Realizar exéresis completa si fracaso de tratamiento médico (trayectos fistulosos crónicos o ganglios sintomáticos residuales) |
|
Osteoarticular |
H 6 m + R 6 m + Z 2 m + E/aminoglucósido |
Recomendado en compresión medular |
Si a pesar del tratamiento médico se produce empeoramiento clínico, persistencia de la clínica neurológica o inestabilidad articular o espinal |
|
Pericarditis |
H 6 m + R 6 m + Z 2 m + E/aminoglucósido |
Controvertido. Emplear si derrame o pleocitosis importante, pericarditis constrictiva |
Si hay inestabilidad hemodinámica: pericardiocentesis±drenaje externo. Si pericarditis constrictiva: pericardiectomía |
|
Abdominal |
H 6 m + R 6 m + Z 2 m + E/aminoglucósido |
Controvertido. Valorar si complicaciones |
Evitar en lo posible. Reservar para casos de estenosis, perforación localizada, fístulas o sangrado |
|
Genitourinaria |
H 6 m + R 6 m + Z 2 m + E/aminoglucósido |
Controvertido. Valorar si complicaciones |
Si hay hidronefrosis secundaria a estenosis uretral: drenaje externo. Riñón no funcionante: nefrectomía |
|
Pleural |
H 6 m + R 6 m + Z 2 m + E/aminoglucósido |
Controvertido, beneficio en caso de gran derrame o fiebre |
Toracocentesis repetidas si derrame masivo o con afectación clínica. Tubo de drenaje si fístula broncopleural o empiema |
|
Endobronquial |
H 6 m + R 6 m + Z 2 m + E/aminoglucósido |
Recomendado |
|
H: isoniacida. R: rifampicina. P: pirazinamida. E: etambutol
-
Tratamiento de la enfermedad tuberculosa6
- Tuberculosis pulmonar
En nuestro medio, y debido a la tasa de resistencia ≥ 4%, la pauta de elección de inicio sin conocer sensibilidad de la cepa fuente, será con 4 fármacos: isoniacida (H) + rifampicina (R) + pirazinamida (P) + etambutol (E) en la fase de inicio (duración 2 meses); y con 2 fármacos (HR) durante la fase de mantenimiento (4 meses). Dosis en la (Tabla 6)
Puntualizaciones:
- El cuarto fármaco debe suspenderse siempre que se conozca la sensibilidad de la cepa (del caso índice)
- El cuarto fármaco más empleado es etambutol (E) por vía oral, en el que se debe vigilar la aparición de neuritis óptica (agudeza visual y distinción entre color rojo-verde). Una alternativa, de uso excepcional, son los aminoglucósidos, como amikacina o estreptomicina.
- Los fármacos deberán tomarse juntos y en ayunas
- Los pacientes con comorbilidades o toma concomitante de otros fármacos, se deben remitir a unidades especializadas
Este tratamiento consigue curación en más del 95% casos, con escasos efectos adversos
- Tuberculosis extrapulmonar6 (Tabla 7)
-
Seguimiento6
A) Seguimiento ITBL:
El bajo riesgo de hepatotoxicidad en niños desaconseja realizar controles rutinarios de función hepática durante el tratamiento de ITBL, salvo si aparece clínica de hepatotoxicidad, enfermedad hepática de base o recibe medicación hepatotóxica concomitante.
B) Seguimiento TBC:
Analítica basal con transaminasas pre-tratamiento y posteriormente, valorar a las 2-3 semanas o antes si hay clínica.
Casos con buena evolución sin enfermedad pulmonar extensa: control radiológico al final de la fase de inicio y al terminar el tratamiento.
Casos con hipoventilación, sibilancias focales, enfermedad extensa, cavitación, derrame, incumplimiento o resistencia farmacológica: estudio de imagen o fibrobroncoscopia cuando sea preciso.
En los primeros 2 meses de tratamiento, puede aparecer reacción paradójica en un 5-10% de los casos, caracterizada por un empeoramiento clínico-radiológico. En estos casos se asociarán corticoides orales 2 mg/kg/día de prednisona o equivalente, durante 3-4 semanas, con descenso progresivo en 2 semanas.
Tras el alta domiciliaria (si el ingreso fue necesario) y asegurado el cumplimiento, esperar unos días de convalecencia para incorporarse a la actividad normal, manteniendo el aislamiento respiratorio hasta que los resultados de esputo sean negativos.
-
IGRAs
Los Interferón-Gamma Release Assays (IGRAs), son test que detectan la producción de interferón gamma (IFNγ) por linfocitos T sensibilizados frente a micobacterias tuberculosas (MT). La principal diferencia entre PT e IGRAs es que mientras el primero utiliza PPD, una mezcla de antígenos comunes a distintas especies de micobacterias, los IGRAs utilizan antígenos más específicos de MT: Early Secreted Antigenic Target-6 (ESAT-6), Cultured Filtrated Protein-10 (CFP-10) y TB 7.7. Estos antígenos, sin embargo, no son completamente exclusivos de MT y se encuentran también en algunas micobacterias no tuberculosas (MNT) (M. szulgai, M. marinum y M. kansasii). Por lo tanto, aportan mayor especificidad7. Estos antígenos tampoco se encuentran en la BCG. El periodo de ventana de los IGRAs es de unas 4-8 semanas, muy similar al del Mantoux.
Actualmente existen 2 tipos de test: el quantiferón TB (QFT-PLUS) que permite detectar y cuantificar de forma separada el IFNγ liberado por los linfocitos CD4 y CD8 del paciente y el T-SPOT.TB, que permite cuantificar el número de células productoras de interferón. En nuestro medio el QFT-PLUS es el test más usado; posiblemente porque técnicamente el T-SPOT.TB requiere más sangre, mayor tiempo de preparación, es más laborioso de realizar y además no permite trabajar con las muestras de manera diferida7.
INDICACIONES
Paciente sin factores de riesgo:
La PT sigue siendo el test de elección en el cribado de la ITBL. Si el Mantoux es negativo y el paciente no tiene factores de riesgo, es inmunocompetente y/o el tipo de contacto es de baja prioridad: no hay indicación de IGRA, puesto que la sensibilidad de estos test es similar a la del Mantoux1,9,10,11. La IDSA (Infectious Diseases Society of America), en un reciente documento propone realizar IGRAs en lugar de PT en mayores de 5 años con historia de vacunación con BCG y riesgo de pérdida del paciente8.
Se debe realizar un IGRA en los casos de Mantoux positivo en los que sea preciso descartar que se trate de un falso positivo, como serían, la vacunación previa con BCG, exposición a micobacterias no tuberculosas (MNT), infección o hematoma en zona de inoculación o alergia a otros componentes del PPD.
Paciente con factores de riesgo:
En pacientes con factores de riesgo de desarrollar una enfermedad tuberculosa, puede valorarse su uso para aumentar la especificidad del estudio (ej. pacientes alto riesgo y Mantoux negativo o dudoso) tanto en mayores de 5 años, como incluso en mayores de 3 años8,10. Estos pacientes deben de ser evaluados por pediatras con experiencia9.
Los principales factores de riesgo para el desarrollo de la enfermedad son: ser contacto de alta prioridad (Tabla 2 y 3), la infección reciente (menos de dos años tras la primoinfección), y la presencia de otras comorbilidades o tratamientos que alteren la inmunidad4,9.
NEGATIVO[M]
-
Prueba de IGRA positiva
Se considera que el resultado del ensayo QFT-PLUS es positivo si la producción de IFN-γ como reacción a cualquiera de los tubos de antígeno TB es claramente superior al valor en UI/ml de nulos para IFN-γ.
-
Prueba de IGRA indeterminada
Los resultados indeterminados son poco habituales y pueden estar relacionados con el estado inmunológico del individuo o con diversos factores técnicos (Ver ficha técnica: https://www.sergas.es/Docs/Avalia-t/avalia-t200901-1-interferongamma.pdf).
En los casos indeterminados, se recomienda evaluar el riesgo individualizado y mantener un seguimiento estrecho si finalmente se decide no iniciar profilaxis primaria.
-
Prueba de IGRA negativa
Un resultado negativo del QFT-PLUS no descarta totalmente la posibilidad de una infección por MT. Los falsos negativos pueden deberse a la etapa de la infección en que se encuentre el paciente (p. ej. si la muestra se ha obtenido antes de que se desarrolle la respuesta celular inmune), enfermedades asociadas que afecten al mecanismo inmunológico, a una incorrecta manipulación de los tubos de recogida de sangre después de la venopunción, a una realización errónea del ensayo o a otras variables inmunológicas (Ver ficha técnica: https://www.sergas.es/Docs/Avalia-t/avalia-t200901-1-interferongamma.pdf).
en 8-12 semanas
-
Radiografía (Rx) de tórax
Todas las guías coinciden en la importancia de la Rx de tórax en el diagnóstico de la tuberculosis y que debe realizarse en todos los niños con sospecha de tuberculosis1,11. Sin embargo, la lectura de la Rx es muy subjetiva y el patrón de presentación variable, por lo que su sensibilidad y especificidad son bajas1,11.
Los pacientes menores de 3-4 años tienen mayor afectación de los ganglios linfáticos, pero menor afectación parenquimatosa que los niños más mayores, por lo que el papel de la Rx de tórax es menor en niños pequeños y la Rx lateral no mejora su rendimiento12. No obstante, las guías españolas aconsejan realizar, en niños, radiografía de tórax frontal y lateral6.
- Si la Rx de tórax es normal, el paciente está asintomático y no existen factores de riesgo de progresión (edad, inmunosupresión, contacto con paciente bacilífero muy cercano) se considerará como ITBL.
- Si la Rx es compatible con tuberculosis, dado el alto riesgo de progresión en la edad pediátrica (sobre todo en menores de 5 años) y lo poco específico de la clínica, se continuará estudio con recogida de muestras, TAC si existen factores de riesgo o se considerara necesario y se iniciaría tratamiento de enfermedad tuberculosa. En caso de adenopatías mediastínicas, se debe individualizar el tratamiento en función del riesgo de progresión.
Pruebas microbiológicas[Q]
-
Valoración clínica del paciente. Pruebas microbiológicas6
La presentación clínica de la enfermedad TBC es muy variable, desde formas asintomáticas hasta formas diseminadas, pudiendo afectar a cualquier órgano o sistema, y siempre es necesario un alto grado de sospecha.
La inmunidad celular es el componente fundamental en la forma de presentación y condiciona el riesgo de diseminación, el cual es más elevado a menor edad del paciente.
En inmigrantes de países endémicos de hepatitis virales o de VIH, se deben descartar coinfecciones antes de iniciar tratamiento.
Rentabilidad de las pruebas microbiológicas:
- Baciloscopia de jugo gástrico/esputo (30-40%)
- 80% en lactantes con enfermedad endobronquial avanzada
- Cultivo de esputo inducido/aspirado nasofaríngeo o jugo gástrico (misma sensibilidad 30-40%)
- Cultivo medio sólido (Lowenstein): Resultado en 4-6 semanas
- Cultivo medio líquido (BACTEC): Mayor rapidez: 2-3 semanas
- PCR en tejidos y fluidos (50-60%). Mayor rentabilidad con pruebas repetidas. Sensibilidad similar o algo mayor que baciloscopia. Aumenta rapidez diagnóstica: < 7 días. Permite estudio de sensibilidad a INH y rifampicina
En todos los aislamientos es obligado realizar estudio de resistencias
-
TAC
La tomografía axial computarizada (TAC) es más sensible y específica que la Rx de tórax, y puede demostrar en un gran número de casos con Mantoux/IGRAs positivos, afectación hiliar y/o parenquimatosa1,12. No obstante, el valor de estos hallazgos es controvertido12.
Considerando su alto nivel de radiación, sólo debería utilizarse para el estudio de formas complicadas (ver el punto 4 de los siguientes)1,11; o de acuerdo al documento de consenso de la SEIP y de la sociedad neumología pediátrica (SENP)1y otros autores11, en los siguientes supuestos:
- Niño asintomático, con contacto bacilífero conocido, prueba de tuberculina positiva y radiografía de tórax dudosa o no concluyente
- Niño sintomático, con contacto bacilífero, prueba de tuberculina positiva y radiografía de tórax normal
- Niños inmunodeprimidos con contacto bacilífero conocido y radiografía de tórax normal, independientemente del resultado de la prueba de tuberculina
- Niños con complicaciones o en circunstancias especiales:
- Adenopatías compresivas
- Áreas de atrapamiento aéreo o atelectasia
- Cavitaciones
- Bronquiectasias
- Fístulas broncopleurales
La recomendación es débil, por existir menor evidencia en:
- Niños menores de 2 años asintomáticos con contacto bacilífero conocido, prueba de tuberculina positiva y radiografía de tórax normal
- Niños asintomáticos con contacto bacilífero conocido multirresistente, prueba de tuberculina positiva y radiografía de tórax normal
TRATAMIENTO[P]
SEGUIMIENTO[S]
-
Infección tuberculosa latente (ITBL). Tratamiento
Se define ITBL aquella situación en la que se detecta en un niño asintomático, un Mantoux o IGRAs positivos en un estudio de contactos y tiene una Rx de tórax normal.
La quimioprofilaxis o tratamiento de la ITBL se fundamenta en que está demostrado que el tratamiento con isoniacida (INH) durante un periodo variable (6-12 meses) reduce el riesgo de progresión a enfermedad en un porcentaje en torno al 80%, en función de la duración de la misma, y que esta protección se prolongará más allá de 20 años13.
Todos los niños y adolescentes con este diagnóstico, deben recibir tratamiento6,9,13.
El tratamiento de elección en nuestro medio es INH 10 mg/Kg/día en una dosis diaria (máximo 300 mg) durante 6 meses6,9,13. En pacientes en los que se sospeche una mala adherencia al tratamiento, inmunodeprimidos o con enfermedades crónicas, se aconseja prolongar siempre hasta 9 meses el tratamiento de la ITBL6.
Otras alternativas:
- INH y rifampicina durante 3 meses. Esta pauta está especialmente recomendada en adolescentes o ante sospecha de mala adherencia6,11,13.
- Rifampicina 15 mg/Kg/día en una dosis (máximo 600 mg) durante 4 meses en caso de resistencia a INH o imposibilidad para su uso6,11,13.
-
Seguimiento6
A) Seguimiento ITBL:
El bajo riesgo de hepatotoxicidad en niños desaconseja realizar controles rutinarios de función hepática durante el tratamiento de ITBL, salvo si aparece clínica de hepatotoxicidad, enfermedad hepática de base o recibe medicación hepatotóxica concomitante.
B) Seguimiento TBC:
Analítica basal con transaminasas pre-tratamiento y posteriormente, valorar a las 2-3 semanas o antes si hay clínica.
Casos con buena evolución sin enfermedad pulmonar extensa: control radiológico al final de la fase de inicio y al terminar el tratamiento.
Casos con hipoventilación, sibilancias focales, enfermedad extensa, cavitación, derrame, incumplimiento o resistencia farmacológica: estudio de imagen o fibrobroncoscopia cuando sea preciso.
En los primeros 2 meses de tratamiento, puede aparecer reacción paradójica en un 5-10% de los casos, caracterizada por un empeoramiento clínico-radiológico. En estos casos se asociarán corticoides orales 2 mg/kg/día de prednisona o equivalente, durante 3-4 semanas, con descenso progresivo en 2 semanas.
Tras el alta domiciliaria (si el ingreso fue necesario) y asegurado el cumplimiento, esperar unos días de convalecencia para incorporarse a la actividad normal, manteniendo el aislamiento respiratorio hasta que los resultados de esputo sean negativos.
-
EXPOSICION TUBERCULOSA. Fundamentos de la profilaxis primaria / tratamiento de contactos
Definición: Exposición a tuberculosis sin signos de infección con primer Mantoux o IGRA negativo
No existe un acuerdo sobre la profilaxis primaria en estos casos. La mayoría de los autores proponen iniciar tratamiento, dado el mayor riesgo de desarrollar enfermedad durante el periodo ventana en:
- Menores de 5 años.
- Pacientes inmunodeprimidos (tratamientos inmunosupresores, comorbilidades, inmunodeficiencias) de cualquier edad.
En el resto de los pacientes puede obviarse el tratamiento, manteniendo una estrecha vigilancia hasta la realización del segundo Mantoux o IGRA6 .
La profilaxis primaria se realiza con isoniacida (INH) a 10mg/kg/día (dosis máxima: 300mg) + piridoxina hasta repetir el Mantoux a las 8-12 semanas, puesto que el periodo ventana oscila entre 4-12 semanas:
- Si este es negativo (<5 mm) se suspenderá el tratamiento en aquellos en los que se había iniciado. Aunque sea negativo, en menores de 3 meses o inmunodeprimidos con contacto de alto riesgo se aconseja completar tratamiento de ITBL6 (P) por ser pacientes de alto riesgo en los que el valor del Mantoux tiene bastantes limitaciones.
- Si es positivo (>5 mm) se continuará con la evaluación del paciente, realizando una radiografía de tórax (N).
