

Ronquido nocturno
TABLA 1. Cuestionario BEARS
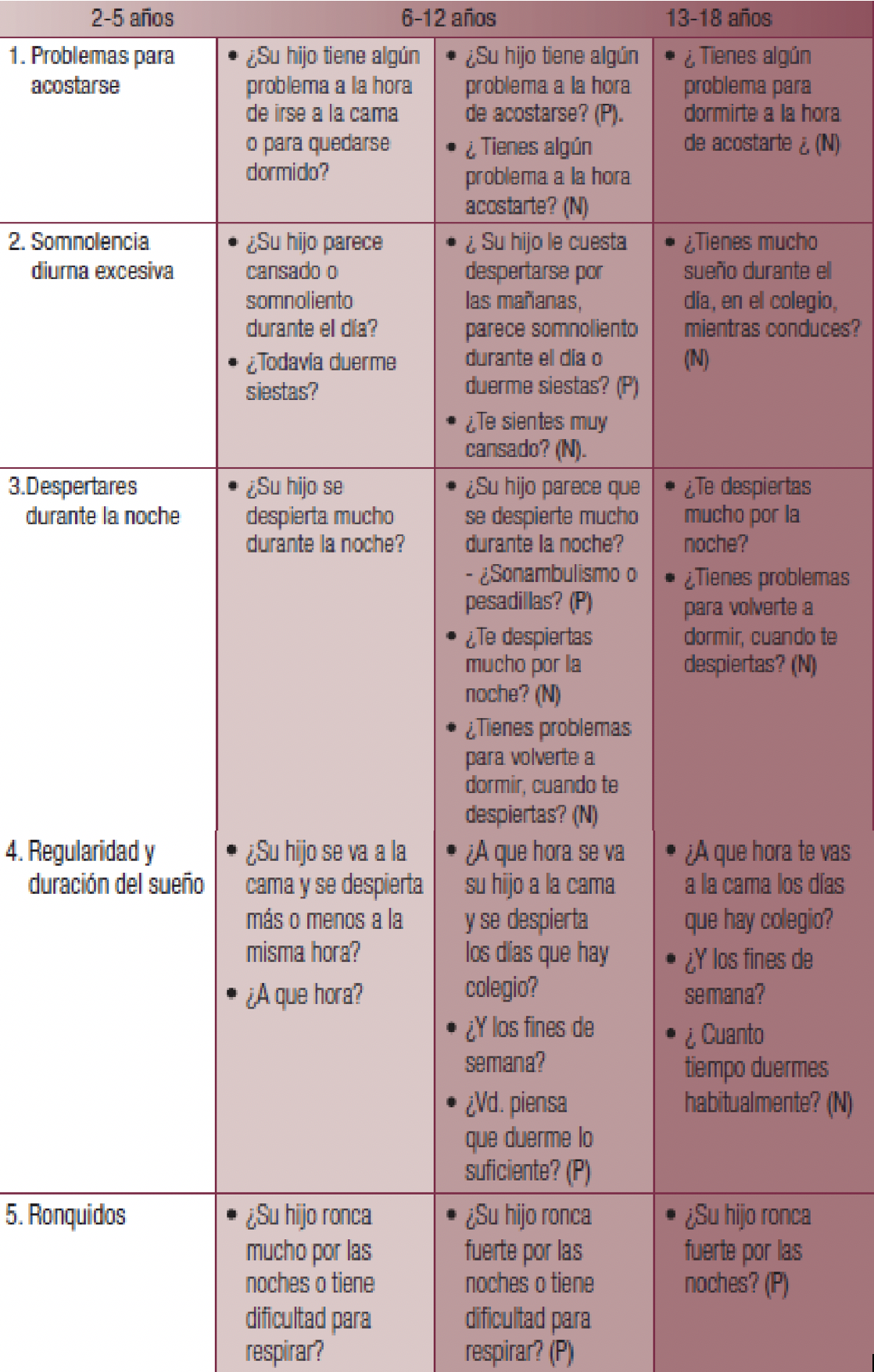
Con una respuesta positiva se recomienda profundizar más en el estudio de sueño, realizando en primer lugar el cuestionario SCDC de Bruni y dependiendo de cúal sea la sospecha algún otro estudio. Si normal se descarta el 90% de problemas de sueño infantil
-
Niño roncador habitual:
Es aquel que ronca más de 3 veces por semana durante más de 3 semanas consecutivas sin que presente un cuadro catarral de vías altas y/o rinitis acompañante1,2.
El ronquido es el síntoma cardinal de los denominados trastornos respiratorios del sueño (TRS) que engloban 4 entidades en un espectro continuo3:
- Ronquido simple o primario: ruido respiratorio durante el sueño sin apneas, hipoventilación ni alteraciones en la estructura del sueño ni en el intercambio de gases: antes llamado ronquido benigno, ahora se sabe que tiene efectos en el desarrollo neurocognitivo y sobre la tensión arterial. Lo presentan aproximadamente un 5-15% de los niños y adolescentes1.
- Síndrome de resistencia aumentada de la vía aérea superior (SRAVAS): caracterizado por episodios recurrentes de obstrucción de la vía aérea en ausencia de apneas o hipopneas y de alteraciones en el intercambio de gases, pero con microdespertares relacionados con el esfuerzo respiratorio que fragmentan el sueño.
- Síndrome de hipoventilación obstructiva: ronquido con una presión parcial de CO2 en aire espirado elevada en ausencia de eventos obstructivos reconocibles.
- Síndrome de apnea/hipopnea del sueño (SAHS): ausencia total o parcial del flujo aéreo nasal y oral que se produce de forma intermitente durante el sueño, con una duración de al menos el doble de un ciclo respiratorio, en presencia de una actividad y esfuerzo muscular torácico y abdominal y que ocasiona una desaturación de oxígeno con o sin retención de CO2 y que altera el patrón normal del sueño. Afecta a un 2-4% de los niños y adolescentes4.
-
Circunstancias que incrementan el riesgo de presentar ronquido3,4:
Obesidad, fallo de medro, hipertensión arterial, prematuridad, S Down y otros síndromes dismórficos craneofaciales (acondroplasia, S. Crouzon, S. Apert, secuencia Pierre Robin, S. Treacher-Collins y otros) , tabaquismo pasivo, patología respiratoria (asma, rinitis, fibrosis quística, laringomalacia), transtornos neuroconductuales ( TDAH, depresión, ansiedad, epilepsia), bajo rendimiento escolar, enuresis nocturna, excesiva somnolencia diurna, antecedentes familiares de SAOS y/o de necesidad de adenoamigdalectomía, preocupación de los padres en relación a la respiración del hijo durante el sueño, hipertrofia adenoamigdalar, OMA de repetición, trastornos neuromusculares ( parálisis cerebral infantil, distrofia muscular de Duchenne).
-
CRITERIOS CLÍNICOS DE SAHS del Consenso Nacional de SAHS infantil1:
Mayores: problemas de aprendizaje, somnolencia diurna (se duerme en clase más de una vez por semana), conducta TDAH, Presión arterial > P85 para la edad y talla, enuresis nocturna resistente al tratamiento, obesidad (IMC>p97 para la edad), hipertrofia adenoidea y amigdalar (índice de Mallampatti > 2).
Menores: hipercolesterolemia, otitis media y/o resfriados de repetición, asma y/o rinitis alérgicas, antecedentes familiares de SAOS (en al menos un progenitor o en 3 familiares cercanos) y antecedentes personales de prematuridad.
La existencia de al menos 4 criterios mayores o bien de 3 criterios mayores y 2 menores sugiere fuertemente la existencia de un SAHS.
Existe una dificultad evidente a la hora de valorar alguno de los criterios en los niños menores de 5 años (p.ej la somnolencia diurna y la enuresis).
-
VALORACIÓN CLINICA.
Hallazgos en la exploración física que apoyan la existencia de un posible trastorno respiratorio del sueño: facies adenoidea, paladar ojival, retro/micrognatia, maloclusión dentaria, macroglosia.
Se deben valorar la existencia de antecedentes traumáticos faciales que puedan hacernos sospechar la existencia de desviaciones septales o septopiramidales obstructivas así como el grado de hipertrofia adenoamigdalar5. Es preciso recalcar que dicho grado de hipertrofia no está directamente relacionado con la existencia y la gravedad del SAHS: amígdalas pequeñas no lo excluye ni amígdalas y adenoides de gran tamaño lo aseguran.
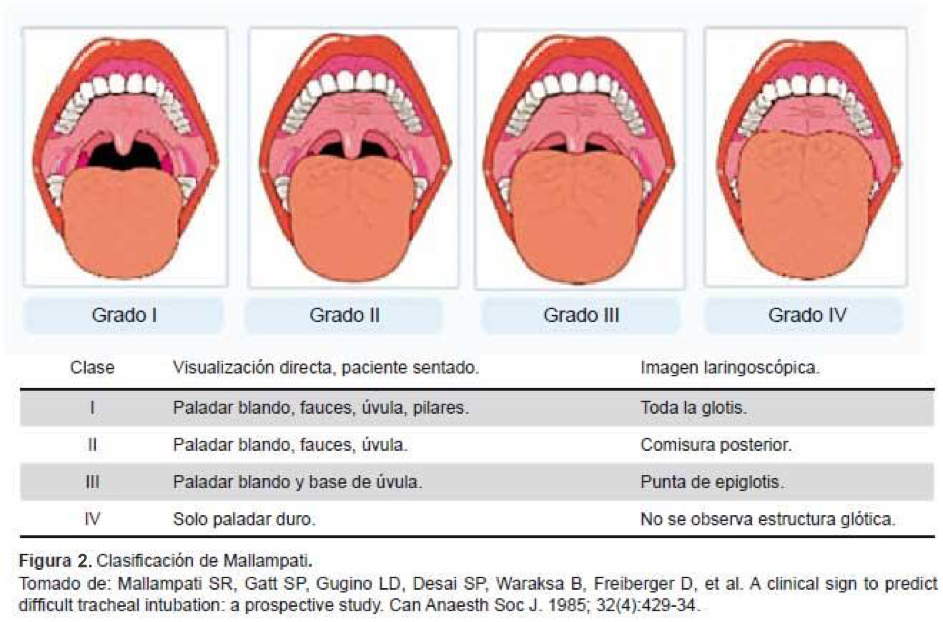
Como herramientas de ayuda para valorar el tamaño amigdalar6 pueden usarse la escala de Friedman (Figura 1) o la de Mallampatti (Figura 2).
En la valoración del tamaño adenoideo se recomienda en la actualidad la visión directa de la vía aérea superior mediante fibroendoscopio flexible7que supera las limitaciones técnicas y de interpretación de la clásica radiografía lateral de cavum8.
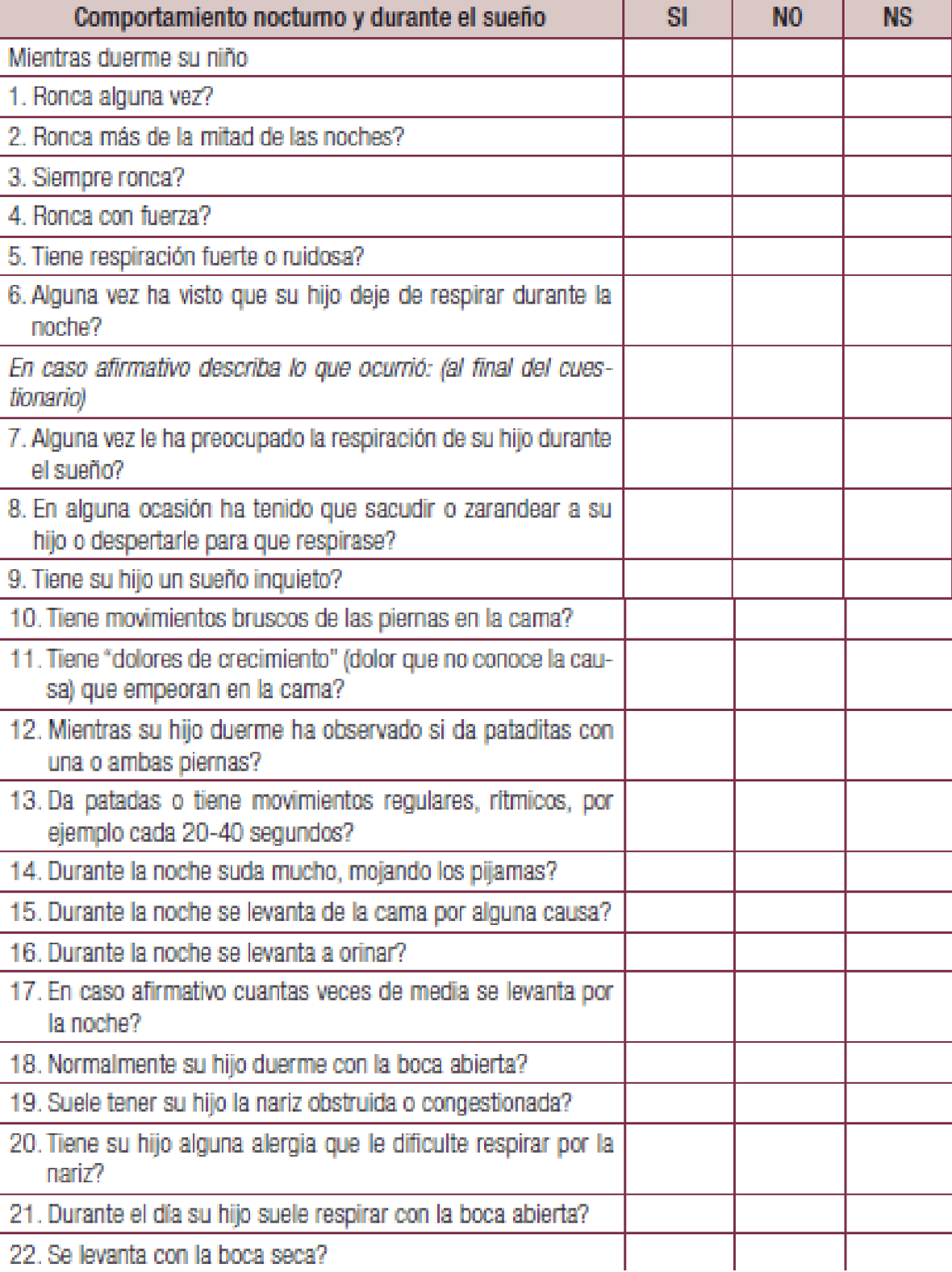
En la valoración clinica de los pacientes roncadores entre 2 y 18 años de edad contamos con la posibilidad de usar el Pediatric Sleep Questionnaire de Chervin orientado al SAHS9,10: el resultado de más de un 33% de respuestas positivas indica la existencia de un SAHS con una sensibilidad del 78% y una especificidad del 72%3 (Tabla 2).
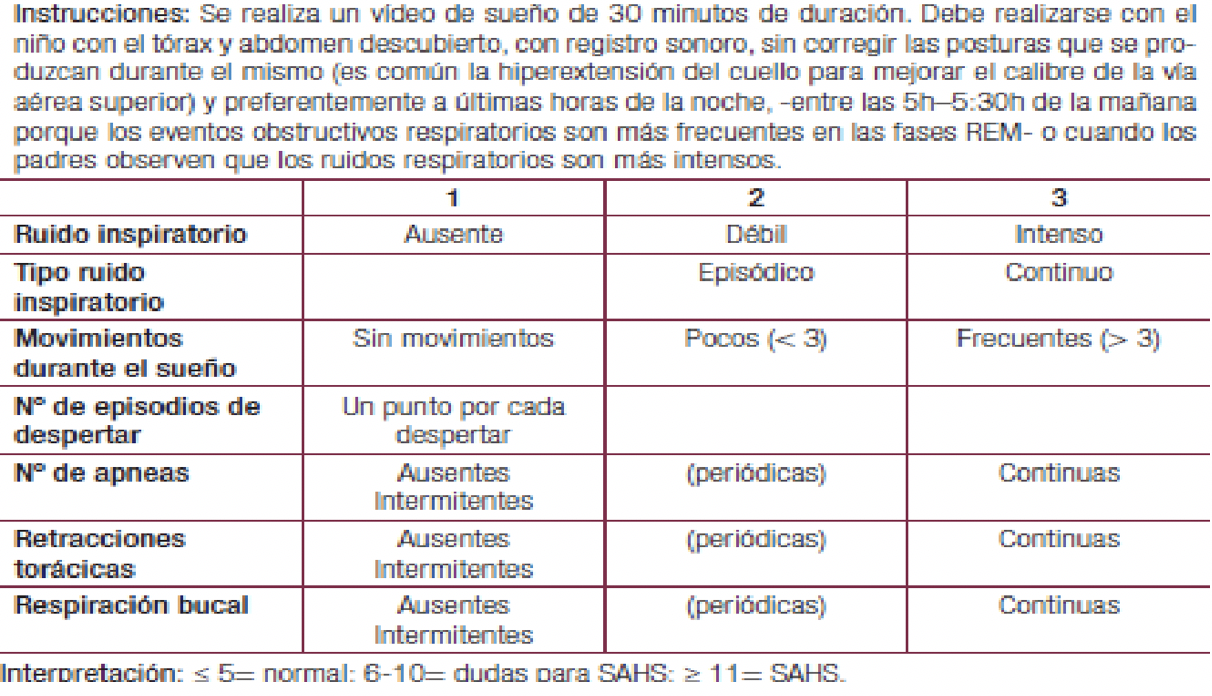
Podemos además solicitar una videograbación domestica del sueño de aquellos niños que roncan y presentan un PSQ de Chevin significativo: la grabación se valora mediante la puntuación de Sivan 11 que presenta una sensibilidad y una especificad del 89 y el 77%, respectivamente, para el diagnóstico del SAHS. Su punto de corte predice el 55% de los casos de TRS. (Tabla 3)
Figura 1. Escala de Friedman
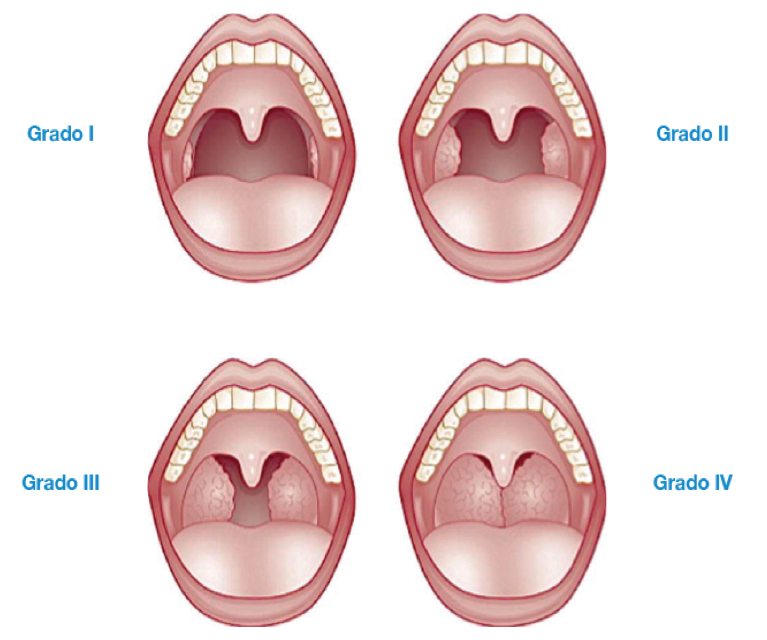
Figura 2. Escala de Mallampatti
CUESTIONARIO PSQ Chervin
(Tabla 2)
Tabla 2. Cuestionario PSQ de Chervin.
VIDEOSCORE DE SIVAN
(Tabla 3)
Tabla 3. Videoscore de Sivan
-
UNIDAD DE SUEÑO O CENTRO DE REFERENCIA:
Lo ideal sería que todo niño con alta sospecha de presentar un SAHS fuera evaluado en una Unidad de Sueño; pero la realidad es que en el momento actual no existen suficientes centros acreditados para poder atender a la totalidad de estos niños, por lo que en el caso de que no existiese dicha posibilidad estos pacientes deberían ser evaluados por un equipo multidisciplinar que podría estar integrado por una Unidad de ORL con experiencia en el manejo de los trastornos respiratorios del sueño y/o una Unidad de Neumología, Neurología y/o Neurofisiología infantil además de por un equipo de odontólogo/ortodoncista/ cirujano maxilofacial infantil, dependiendo de la organización de cada área sanitaria1.
OTRAS PRUEBAS COMPLEMENTARIAS[G]
- PULSIOXIMETRÍA NOCTURNA
- POLIGRAFIA RESPIRATORIA (PR)
- OTRAS
-
Poligrafía respiratoria (PR).
Prueba que incluye la medida de variables cardiorrespiratorias pero no de variables neurofisiológicas, por lo cual no permiten registrar el tiempo de sueño; utiliza el tiempo en la cama como denominador de los distintos índices (apneas, hipopneas, desaturaciones), lo que puede producir falsos negativos al ser el tiempo en la cama mayor que el tiempo de sueño real.
Los resultados de la PR se muestran en índice de eventos respiratorios en cada hora (IER), que se considera normal cuando es inferior a 5.
Validada como método diagnóstico de los TRS en adultos (con una sensibilidad del 97% y una especificidad del 90%), no lo ha sido en niños12.
La poligrafía respiratoria es una técnica de cribado útil en el diagnóstico de los TRS infantiles, especialmente en los pacientes con muy alta o muy baja probabilidad de padecer TRS.
Aquellos pacientes con una probabilidad intermedia, aquellos con morbilidad asociada o los que tengan una alta sospecha clínica y PR normal, deberían someterse a una PSG.
Pulsioximetría nocturna.
Método diagnóstico de fácil implementación, cuando presenta datos anormales (según los Criterios de Mc Gill: al menos un 4% del tiempo total del sueño con desaturaciones de oxígeno, siendo al menos 3 de ellas por debajo del 90%), apoya fuertemente el diagnóstico de SAHS (valor predictivo positivo del 97%). Su alta tasa de falsos negativos y de resultados no concluyentes (valor predictivo negativo del 47%) hace que cuando el resultado es normal no pueda excluirse la posibilidad de un SAHS14.
Otras técnicas diagnósticas:
Como son el estudio cefalométrico15 (especialmente en niños con alteraciones craneomandibulares), la ortopantomografía y otras exploraciones odontológicas16, la faringometría acústica, la fluoroscopia, la resonancia magnética o la tomografía computarizada ultrarrápida o cine-TC que reproduce con precisión las vías respiratorias durante la fase de respiración y períodos de apnea.
POLISOMNOGRAFIA
(PSG)[F]
-
Polisomnografía (PSG) nocturna.
Constituye la prueba patrón oro en el diagnóstico de los trastornos respiratorios del sueño (TRS)1,3,4.
Es una prueba en la que se registran diferentes parámetros fisiológicos durante el sueño. Consiste en el registro simultáneo de variables neurofisiológicas y cardiorrespiratorias y de los eventos cardiacos, neurológicos y motores que acontecen durante el sueño y que pueden afectar a la calidad del mismo. En la polisomnografía convencional se registra la actividad respiratoria durante el sueño mediante neumotacógrafos y termistores que miden el flujo aéreo nasobucal y bandas de sensores de impedanciometría para determinar los movimientos torácicos y abdominales, sensores de ronquidos así como la saturación de oxígeno por pulsioximetría y el nivel de CO2 en el aire exhalado. Las variables no respiratorias que se recogen incluyen la actividad cerebral mediante EEG, la actividad muscular con un electromiograma de superficie habitualmente submentoniano (EMG), los movimientos oculares con un electrooculograma (EOG) y la posición corporal mediante sensores en las extremidades. La actividad cardiaca se recoge mediante un electrocardiograma convencional de 3 derivaciones (ECG). Mediante el EEG se determina si el sujeto está despierto o dormido. El EEG junto al EOG y al EMG sirven para reconocer en qué fase del sueño se halla el paciente.
También se registran el pH y la presión intraesofágica si se sospecha que los síntomas están en relación con un reflujo gastroesofágico y se puede realizar grabación de video sincronizado con la PSG para establecer una correlación electroclínica de cualquier evento que acontezca durante el sueño.
Para que sea valorable, el registro polisomnográfico estándar debe de abarcar un periodo nocturno (o en el horario habitual de sueño del paciente) de al menos 6,5 horas, con al menos 180 minutos de sueño. La PSG durante la siesta sólo es válida cuando avala el diagnóstico de SAHS pero ante un resultado negativo y clínica sugestiva se recomienda realizar una PSG de sueño nocturno.
La PSG es una prueba costosa tanto económica como metodológicamente ya que requiere de un material y un personal muy especializados para su realización e interpretación. Además, carece de unos criterios estandarizados y validados universalmente para la valoración de los TRS.
La PSG está especialmente indicada en la evaluación de un posible SAHS cuando el paciente presenta obesidad, deformidades craneofaciales, trastornos neuromusculares, o alteraciones complejas (del tipo de S Down, S Prader-Willi, malformación de Arnold Chiari), cuando la necesidad del tratamiento no está clara y siempre antes de realizar tratamientos de cirugía maxilofacial u ortodoncia o de instaurar tratamiento con presión positiva de la vía aérea3.
Los resultados de la polisomnografia se muestran como índice de apneas/hipopneas por cada hora (IAH). Se acepta como normal un IAH inferior a 1-2 eventos en cada hora (aunque puntuaciones superiores son estadísticamente anormales pero no implican que sean clínicamente significativos)3.
Cuando el IAH se sitúa entre 1 y 3 sería de dudosa significación clínica, aceptándose que aquellas puntuaciones de IAH entre 3 y 5 corresponderían a SAHS leve, IAH entre 5 y 10 a SAHS moderado y las superiores a 10 a SAHS grave1.
- IAH <3
- IAH 3-5 SIN COMORBILIDADES
-
ADENOAMIGDALECTOMIA (AA).
Es el procedimiento terapeútico más frecuentemente realizado1,4. En niños con SAHS documentado e hipertrofia sólo adenoidea, algunos autores aconsejan realizar también amigdalectomía, ya que la severidad del SAHS no se correlaciona necesariamente con el tamaño de las amígdalas3.
Con respecto a la mejor técnica quirúrgica, la última Revisión Cochrane llega a la conclusión de que ninguna técnica de amigdalectomía (extracapsular, subcapsular o total frente a amigdalectomía intracapsular, parcial o amigdalotomía) ha demostrado que sea la más eficaz, y sólo la amigdalotomía parece ser que tenga menor morbilidad que la amigdalectomía17.
Las complicaciones quirúrgicas postoperatorias en la adenoamigdalectomía en el SAHS infantil son mayores que en otras cirugías, recomendándose monitorización en el postoperatorio en los casos de mayor riesgo1: edad menor de 3 años, anomalías craneofaciales, retraso de crecimiento, obesidad, parálisis cerebral, cor pulmonale o graves alteraciones en el estudio polisomnográfico previo a la intervención quirúrgica (IAH> 25, desaturaciones graves por debajo del 80% e hipercapnia con valores superiores al 60 %). Se recomienda en estos casos hospitalización y monitorización continua con pulsioximetría durante al menos la primera noche del tratamiento quirúrgico4, pudiéndose utilizar la presión positiva continua en la vía aérea (CPAP) en el período perioperatorio para estabilizar a los pacientes antes de la cirugía y para tratamiento de las complicaciones postoperatorias3 .
Aunque se estima que su eficacia en la resolución del SAHS es del 70-80%, son necesarios estudios aleatorizados, a doble ciego, y con controles, para conocerla con certeza17.
-
FACTORES DE RIESGO DE RECURRENCIA DEL SAHS.
Se sabe que la persistencia y recurrencia es mayor en niños que presentan SAHS grave (IAH>10), obesidad, síndrome de Down, anomalías craneofaciales y alteraciones neuromusculares (parálisis cerebral infantil)3.
En estos casos se recomienda la realización de una PSG de control a los 3-6 meses de la intervención1.
El resto de pacientes intervenidos sin comorbilidad pueden ser controlados en la consulta de pediatría de atención primaria vigilando la reaparición de sintomatología del SAHS y con la realización periódica del cuestionario PSQ de Chervin cada 6-12 meses.
-
TRATAMIENTO MÉDICO
No supone, generalmente, el tratamiento de elección de primera línea. Hay estudios prometedores con corticoides intranasales27 y con antagonistas de los receptores de los leucotrienos 28, pero se requieren más ensayos clínicos para demostrar su efectividad y para conocer sus efectos a largo plazo.
Podrían ser sus indicaciones los casos de SAHS leve: IAH entre 1 y 3, o incluso aquellos con IAH entre 3 y 5 sin comorbilidad, sin obesidad, alteraciones craneofaciales ni trastornos neuromusculares, con hipertrofia adenoidea moderada- grave y predominancia de síntomas nasales1.
-
OTROS TRATAMIENTOS QUIRÚRGICOS.
En casos seleccionados con alteraciones anatómicas de la morfología maxilofacial o en aquellos SAHS que no han respondido al tratamiento de AA y/o a la presión positiva continua (CPAP) puede ser preciso realizar septoplasta, uvulopalatoplastia, epigotoplastia, glosoplexia, cirugía ortodóncica, o de avance maxilofacial mediante distracción-osteogénesis18,19 .
La traqueotomía, a pesar de que es de una alta eficacia en el tratamiento del SAHS que no ha respondido a otros tratamientos, sólo se usa en casos muy seleccionado debido a las evidentes limitaciones en la calidad de vida de los pacientes que produce3.
-
OTROS TRATAMIENTOS QUIRÚRGICOS.
La CPAP consiste en una turbina que transmite el aire a una presión predeterminada y constante a través de una mascarilla nasal adaptada a la cara del sujeto durante el sueño nocturno. Así se transmite la presión positiva a toda la vía aérea superior e impide su colapso, tanto estático (apneas) como dinámico (hipopneas) durante el sueño20.
La primera información acerca del uso de la CPAP en niños fue en 1984, cuando Schmidt-Nowara describió un caso único en el que el tratamiento con CPAP se utilizó con éxito durante 1 año. Hoy el tratamiento con CPAP está considerado, tras la AA como la segunda opción para la población pediátrica que padece SAHS21.
A diferencia del adulto, a quien se prescribe la CPAP como primera opción a los pacientes con SAHS moderado y severo, en el caso de los niños el uso de la CPAP queda más restringido a una población concreta: SAHS residual tras AA, SAHS relacionado con la obesidad, con alteraciones craneofaciales o trastornos neuromusculares, en casos que no pueden ser intervenidos quirúrgicamente, en el tiempo de espera hasta la intervención quirúrgica y para estabilizar a ciertos pacientes tantos en el pre como en el postoperatorio3.
La presión óptima es la mínima necesaria para evitar el colapso de la vía aérea que evite la aparición de complicaciones y provoque el menor disconfort posible; suele oscilar entre 4 y 6 cm de H2O.
Aunque se ha documentado su eficacia y seguridad en pacientes de todas las edades (desde prematuros22 hasta adolescentes), la FDA sólo autoriza su uso a niños de más de 7 años y 30 kg de peso23.
Para la titulación de dicha presión es imprescindible la realización de una PSG nocturna que permita comprobar la desaparición de los eventos respiratorios y del ronquido, la normalización de la saturación de oxígeno y de los valores de CO2 y la restauración de una adecuada estructura del sueño3.
Es fundamental un seguimiento estrecho y controles (cada 3-6 meses al menos) para ver la presión necesaria y los ajustes de la mascarilla en niños en crecimiento24.
Entre sus efectos secundarios se incluyen la congestión nasal, rinorrea, epistaxis, distensión gástrica y aspiración de alimentos ,maloclusión dentaria, dermatitis facial y en algún caso la posibilidad de hipocrecimiento facial por la presión de la mascarilla25.
El éxito de la terapia con CPAP depende de la tolerancia y de la adherencia al tratamiento, que aumentan mucho con un adecuado entrenamiento y apoyo a los padres y al pacienteundefined.
